�ɂ��M��ˎ����ͣ�M�ڡ�
���@��ˎ��ͣ�M��
3��25�գ�����ˎ�O�ְl�����P�ڌ�ӡ�Ȱ��°�������˾����ԭ��ˎ��ͣ�M��ͨ�P�䰸�Ĺ��棨2019���23̖������

����ˎ�O�ֱ�ʾ�����ڌ�ӡ�Ȱ��°�������˾�M���_չˎƷ�������a�F���z�飬�z��Ʒ�N������ԭ��ˎ���z��l�Fԓ��I�����T�����}������ԭ��ˎ���a�^����׃�������l���Ͳ���ԭ���ϵ�Ͷ������δ�����о���r���҇�ˎƷ�O�ܲ��T����a����Ո�ȡ�
�C���u���J�飬ԓƷ�N���a�������҇���ˎƷ���a�|������Ҏ����2010����ӆ����������ˎ�O�֛Q�����Լ����𣬸��M�ڿڰ�ˎƷ�O�ܲ��T��ͣ�l��ԓ�aƷ���M��ͨ�P�{�C��
��׃�����a��ˇδ���ͣ�M��
ͬ�գ�3��25�գ�������ˎ�O�ְl�����P�ڌ�ӡ�ȷ����_��ˎ��˾��������ԭ��ˎ��ͣ�M��ͨ�P�䰸�Ĺ��棨2019���22̖������

����ˎ�O�ֱ�ʾ�����ڌ�ӡ�ȷ����_��ˎ��˾�M���_չˎƷ�������a�F���z�飬�z��Ʒ�N����������ԭ��ˎ���z��l�Fԓ��I��������������ԭ��ˎ׃���˲������a��ˇ�Ȇ��}���C���u���J�飬ԓƷ�N���a�������҇���ˎƷ���a�|������Ҏ����2010����ӆ����Ҫ��
����ˎ�O�֛Q�����Լ����𣬸��M�ڿڰ�ˎƷ�O���������T��ͣ�l��ԓ�aƷ���M��ͨ�P�{�C��
���@Щ�M��ˎ��������
2018��6��7�գ�����ˎ�O�֛Q����ͣ�N��ʹ��ӡ�������tˎ��������˾���}�ᰱ���� ��Ӣ������AmbroxolHydrochloride���M��ˎƷע���C̖��H20160465����
2018��5��14�գ�����ˎ�O�֛Q����ͣ�N��ʹ��ӡ��̫�ˎ�I����˾��ע���Á���������˾�����c������ԭ���LJ���ˎ�O���T�ں����w�z�r���l�F����z��I����׃�����a��ˇ�����a�h���_����Ҫ��Ȇ��}��
2017��10��31�� ������ʳˎ�O���ְl�����P�ڕ�ͣ�N��ʹ�õ�B.BraunMelsungen AG���L�֬����/�����ᣨ16��/�����ǣ�16%��ע��Һ����-3�~����/�L�֬����ע��Һ�Ĺ��棨2017���127̖������
2017��10��24�գ�����ʳˎ�O���ְl�����P�ڕ�ͣ�N��ʹ�ð���͢TRB PharmaS.A.�������ļ�������֬�c�}ע��Һ�Ĺ��棨2017���123̖������
2017��6��2�գ�����ʳˎ�O���ְl�����P�ڕ�ͣ�N��ʹ�Æ���Һ���ļ�������֬�cע��Һ�Ĺ��棨2017���69̖������
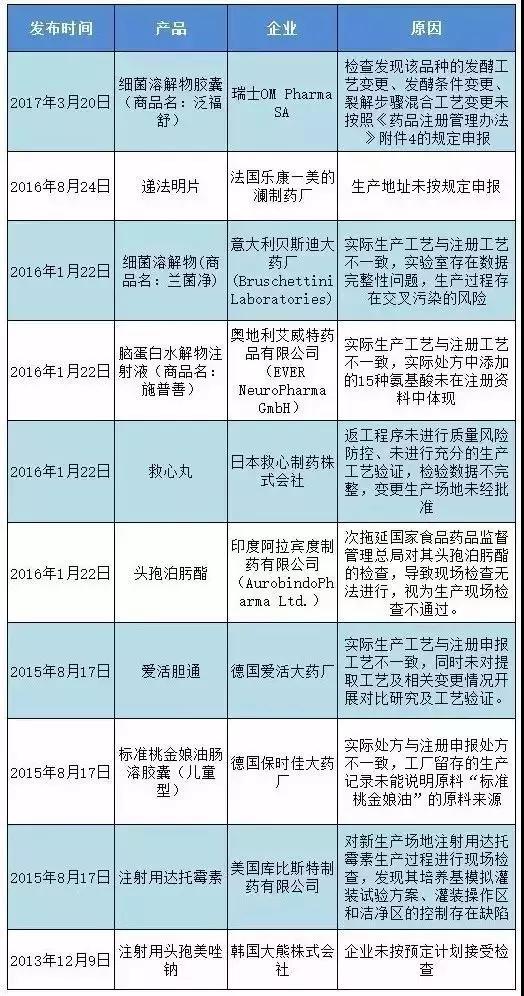
����֮�⣬߀��10��ˎƷ��Ҳ������ֹ�M�ڡ���D��
|